Enterocolitis Necrotizante
La enterocolitis necrotizante es la patología del sistema digestivo adquirida más frecuente y grave en el periodo neonatal, afecta principalmente a recién nacidos prematuros de muy bajo peso al nacer con una incidencia de 1 a 4 por cada 1000 nacidos vivos aproximadamente.
Se estima que en los Estados Unidos representa aproximadamente un 5-7% de los ingresos a las unidades de cuidados intensivos neonatales.
Se define como un proceso isquémico que avanza a necrosis en la mucosa de la pared intestinal generando un estado inflamatorio que en el peor de los casos genera una perforación del órgano. Como consecuencia produce un shock séptico y en el peor de los casos la muerte de los menores que la padecen.
Anatomía patológica e histología
Las principales áreas afectadas por esta patología abarcan el íleon terminal y el colon proximal, en los casos más complicados puede abarcar todo el tubo digestivo.
A nivel macroscópico se observa el intestino dilatado con áreas de necrosis, hemorragia además de bulas que disecan la pared y zonas de perforación.
Histológicamente se observa necrosis coagulativa, congestión, hemorragia, edema de la submucosa, ulceración, micro trombos capilares, bulas de neumatosis principalmente en submucosa y serosa e infiltración bacteriana.
Patogenia
A pesar de los múltiples estudios de la enfermedad la causa de esta sigue siendo desconocida, se considera una enfermedad multifactorial, entre los principales factores de riesgo se encuentran:
- Prematuridad
- Alimentación enteral con fórmula
- Asfixia perinatal
- Restricción crecimiento intrauterino
- Persistencia del conducto arterioso.
- Administración de indometacina, de bloqueadores de los receptores H2
Más recientemente se han visto asociadas mutaciones genéticas entre las que están TNF-alfa, NOD2 y receptores de la IL-4.
Los dos principales factores de esta enfermedad son la prematuridad y la alimentación enteral con fórmula ambos se presentan en un 90% de los pacientes con ECN
La mayor susceptibilidad de los niños prematuros se atribuye a la inmadurez de la motilidad intestinal, de la función digestiva, de la regulación del flujo sanguíneo mesentérico y de aspectos inmunológicos, locales y sistémicos.
- Inmadurez de la motilidad y la capacidad digestiva La motilidad intestinal comienza a aparecer en el segundo trimestre y alcanza cierto grado de madurez en el tercer trimestre de gestación. Los niños prematuros pueden mostrar un patrón inmaduro que se revierte en respuesta a una alimentación enteral. Esta respuesta de maduración frente a los nutrientes puede estar alterada debido a situaciones asociadas a la prematurez como, el retardo de crecimiento intrauterino, asfixia o hipoxia, antenatal o postnatal, que dan lugar a un retraso en la madurez de la motilidad intestinal. La hipomotilidad retrasa la capacidad digestiva del intestino y las moléculas parcialmente digeridas contribuyen a la lesión intestinal.
- Inmadurez de la circulación enteral El organismo prematuro prioriza la perfusión de cerebro y corazón sobre el intestino y los riñones. La circulación inmadura da lugar a la isquemia-hipoxia del tejido, favoreciendo el daño originado por los alimentos no digeridos y el sobrecrecimiento bacteriano.
- Inmadurez de la función de la barrera intestinal En los prematuros, los componentes de la barrera epitelial no están completamente desarrollados. La superficie intestinal solo estará recubierta de un epitelio simple, por lo que se podría alterar y debilitar fácilmente dando lugar a la translocación de gérmenes o toxinas desde el lumen intestinal. Del mismo modo la barrera bioquímica se encuentra inmadura.
- Nutrición Al poseer un sistema inmaduro, la baja capacidad enzimática del prematuro expone al intestino a mayor cantidad de toxinas y alimentos no digeridos. El alimento menos digerido, causa un desarrollo bacteriano y distensión por los gases producto de la fermentación. Del mismo modo, el uso de alimentación parenteral que no provee de nutrientes mediante la vía intestinal puede promover la inflamación intestinal al dar lugar a períodos prolongados de ayuno y favorecer el crecimiento de flora patógena y adversa.
- Inmadurez de la inmunidad innata lo que puede dar lugar a la hipersensibilidad inflamatoria del intestino del pretérmino frente a antígenos bacterianos por colonización. No existe una buena respuesta inmune local intestinal
La alimentación enteral con fórmula, está generando controversia ya que se ha comprobado el beneficio que otorga la leche materna en cuanto al aporte de anticuerpos que disminuyen procesos inflamatorios además de la disminución del crecimiento bacteriano ya que genera un ambiente ácido a nivel intestinal y por último aporte de factores de crecimiento que ayudan a la restauración de la mucosa intestinal dañada con lo que mejora el sistema inmune del paciente.
Como conclusión se ha visto implicada una triada en la patogenia de la ECN, constituida por isquemia intestinal, traslocación bacteriana (prematuridad) y alimentación enteral.
Los microrganismos implicados en la ECN son difíciles de obtener mediante cultivos, solo un cuarto de los cultivos en sangre muestra datos de bacterias que puedan generar el cuadro dentro de los más frecuentes están: Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis, Enterobacter cloacae, Clostridium perfringens, y Pseudomonas aeruginosa, se han visto implicados en algunas infecciones hongos donde el principal es la Cándida la existencia de infección micótica nos habla de una enfermedad más severa.
Manifestaciones clínicas
Los síntomas se presentan durante las primeras 3 semanas de vida y son inversamente proporcionales al peso al nacer y la edad gestacional y el inicio de estos puede ser tanto insidiosa como repentina.
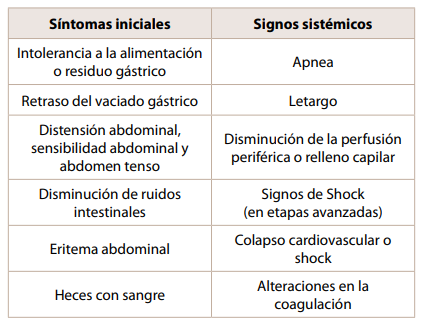
La mayoría de los bebés prematuros que desarrollan ECN generalmente son sanos, se alimentan bien y crecen antes de desarrollar ECN. El signo más frecuente de NEC es un cambio repentino en la tolerancia a la alimentación, que puede manifestarse por numerosos signos clínicos enumerados a continuación. Si bien los residuos gástricos se observan a menudo en la NEC temprana, la comprobación de estos no se realiza tan a menudo, ya que no está bien respaldada por la evidencia actual
Otros signos que presentan ECN incluyen los siguientes hallazgos sistémicos abdominales e inespecíficos:
Los signos abdominales incluyen distensión, residuos gástricos, sensibilidad, vómitos (generalmente biliosos), diarrea, sangrado rectal (hematoquecia) y drenaje biliar de los tubos de alimentación enteral.
Los hallazgos físicos adicionales, que son inespecíficos, incluyen eritema de la pared abdominal, crépitos e induración.
Los hallazgos sistémicos no específicos incluyen apnea, insuficiencia respiratoria, letargo o inestabilidad de la temperatura. La hipotensión resultante de un shock séptico puede estar presente en los casos más graves. Entre el 20% de los lactantes con ECN tienen bacteriemia asociada, lo que puede contribuir a estos hallazgos.
Los hallazgos de laboratorio de los lactantes que presentan ECN a menudo incluyen anemia, trombocitopenia, evidencia de coagulopatía intravascular diseminada (DIC), y en el 20 por ciento de los casos un cultivo sanguíneo positivo, sin embargo, no se observa estrictamente en todos los pacientes afectados.
Se estima que en un tercio de los casos no se logra confirmar la ECN y los síntomas resuelven gradualmente con su tratamiento, sin embargo, entre un 20-40% de los casos presentan una progresión fulminante con signos de peritonitis, perforación intestinal y shock séptico.
Actualmente se utilizan los criterios de la clasificación de Bell, los cuales evalúan el grado de severidad de la ECN.

Diagnóstico
Un diagnóstico definitivo de ECN se hace a partir de muestras quirúrgicas intestinales o post mortem que demuestran los hallazgos histológicos de inflamación intestinal, infarto y necrosis. Sin embargo, para la gran mayoría de los sobrevivientes, no se dispone de un diagnóstico patológico, ya que mejoran con el manejo médico.
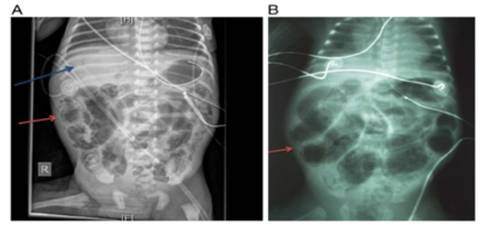
En estos pacientes, hacer un diagnóstico clínico de ECN sigue siendo un reto debido a la falta de un único signo o prueba patognomónica. En general, el diagnóstico clínico se basa en la presencia de los rasgos clínicos más característicos (distensión abdominal, vómitos biliares o aspirado gástrico, y sangrado rectal (heces heme-positivas o muy sangrientas sin fisura anal), y el hallazgo de imágenes abdominales de gas intramuros (neumatosis intestinal), neumoperitoneo o gas hepatobiliar. Aunque las pruebas de laboratorio no se utilizan generalmente para hacer un diagnóstico de ECN debido a su falta de especificidad, se pueden utilizar para apoyar un diagnóstico clínico.
Tratamiento
El tratamiento se debe implementar de manera rápida, para evitar las posibles complicaciones
El mismo brinda medidas de soporte mediante la interrupción de alimentación enteral, descompresión nasogástrica y reposición de líquidos intravenosos, esta última en base a los requerimientos diarios del paciente y tomando en cuenta los hemoderivados.
El soporte cardiaco con inotrópicos, el estado hemodinámico, las correcciones metabólicas y electrolíticas, así como el soporte ventilatorio, se deben considerar de manera conjunta para lograr la estabilidad del paciente.
Se debe iniciar tratamiento antibiótico empírico de amplio espectro los esquemas no deben durar menos de 10 a 14 días, sin embargo, el tiempo del tratamiento va a depender de los cultivos realizados diariamente, los patógenos presentes y la resistencia microbiana.
Las valoraciones físicas frecuentes, el control radiológico con radiografías de abdomen, la determinación del perfil hematológico, electrolítico y metabólico son fundamentales para el manejo de la patología. La posibilidad de un tratamiento quirúrgico se daría ante la presencia confirmada radiológicamente de una extensa área necrótica, una paracentesis abdominal positiva o una perforación intestinal, donde se realiza como primera opción un drenaje peritoneal, sin embargo, se considera laparotomía exploratoria en caso de fallo terapéutico.
Pronóstico y prevención
Según múltiples estudios se han documentado los siguientes posibles métodos preventivos de ECN:
Corticosteroides prenatales: Los corticosteroides prenatales reducen el riesgo de síndrome de dificultad respiratoria (SR) y mortalidad en bebés prematuros. Además, la exposición a corticosteroides prenatales reduce el riesgo de hemorragia intraventricular, retinopatía de prematuridad y ECN. Como resultado, se deben administrar corticosteroides prenatales a todas las mujeres en riesgo de parto prematuro en un plazo de siete días. de la morbilidad respiratoria neonatal y la mortalidad por parto prematuro.
Alimentación de la leche humana: El uso de leche humana reduce el riesgo de ECN en comparación con la fórmula. Siempre que sea posible, se debe utilizar la leche materna y, si no está disponible, se debe utilizar leche humana de donante. No se debe utilizar fórmula bovina.
Los beneficios de la leche humana en comparación con la leche de vaca que se cree que reducen el riesgo de ECN incluyen:
- PH gástrico inferior, mejora la motilidad intestinal, promueve la maduración inmunológica con el suministro de IgA, lactoferrina y oligosacáridos secretarios, reduciendo así el riesgo y el alcance de la disbiosis microbiana.
Evitar el uso prolongado de antibióticos: El microbioma intestinal puede verse alterado por el uso de una terapia antibiótica empírica inicial prolongada, lo que resulta en un mayor riesgo de ECN. Cada día adicional de terapia antibiótica más allá de cinco días se asoció con un aumento adicional de los riesgos de ECN o muerte.
Evitar los bloqueadores de histamina 2: La acidez gástrica puede desempeñar un papel en la prevención de la cascada de eventos infecciosos e inflamatorios que conducen a la ECN. En el neonato, el ambiente de alto ácido regula estrechamente la cantidad de microbios patógenos que coloniza el intestino. Los bloqueadores de H2 como la cimetidina, la ranitidina y la famotidina suprimen la acidez gástrica. Además, la exposición a inhibidores del ácido gástrico también puede estar asociada con un mayor riesgo de neumonía y sepsis.
Probióticos: Probióticos, definidos por la Organización Mundial de la Salud (OMS) como «microorganismos vivos que, cuando se administran en cantidades adecuadas, confieren un beneficio para la salud al huésped,» son una de las medidas preventivas más estudiadas para ECN. Se ha demostrado en una serie de estudios ser eficaz en la prevención de ECN.
En una revisión sistemática de 2017 y metaanálisis de 23 ensayos clínicos, que fueron calificados como de moderada a buena calidad, se observaron los siguientes hallazgos:
- Toda la causa-mortalidad fue menor en el grupo que recibió probióticos en comparación con los controles (4.9 frente a 6.8 por ciento; riesgo relativo [RR] 0.72, 95% CI 0.57-0.92). En los lactantes de muy bajo peso al nacer, sin embargo, no hubo diferencia estadística en la mortalidad (8,9 frente a 14,3 por ciento; RR 0,78, 95% CI 0,50-1,20).
- En un análisis de subgrupos, sólo la combinación de probióticos de Bifidobacterium y Lactobacillus, se encontraron para reducir la ECN y la mortalidad de todas las causas.
Inmunoglobulinas: Las inmunoglobulinas orales pueden reducir la ECN al inhibir la liberación de citoquinas proinflamatorias. Sin embargo, un metaanálisis de cinco ensayos informó de que la administración oral de la combinación de IgG o IgG/IgA no redujo la incidencia de ECN.
Sobre la base de la evidencia disponible, la terapia con inmunoglobulina no debe utilizarse porque hay falta de evidencia que demuestre cualquier beneficio de esta terapia.
Algunas de las complicaciones más comunes o esperadas de la ECN son:
- Obstrucción intestinal por estenosis del intestino delgado y grueso que se presenta en un 10 a 20% de los casos.
- Síndrome de intestino corto.
- Síndrome de malabsorción
- Consecuencias del neurodesarrollo: Pacientes con antecedentes de ECN que han sido tratados quirúrgicamente están en mayor riesgo de problemas desarrollo y problemas de comportamiento. Específicamente crecimiento, retrasos motores y retrasos cognitivos.
Esta revisión fue elaborada a partir de información consultada en diferentes bases de datos disponibles Up to date, Pubmed, Elsevier, Journal of Neonatal-Perinatal Medicine, New England journal of medicine.
Bonilla Cabana, E. et al. Enterocolitis Necrotizante, Medicina Legal de Costa Rica. Available at: https://www.scielo.sa.cr/scielo.php?pid=S1409-00152020000200063&script=sci_arttext (Accessed: 01 June 2024).
Izquierdo, L. G., Sánchez, S. H. C., Bayón, C. S., Díez, R. H., & Iniesta, L. O. (2022). REVISIÓN BIBLIOGRÁFICA Enterocolitis necrotizante en el prematuro. NPunto, 5(55), 127-130.